 |
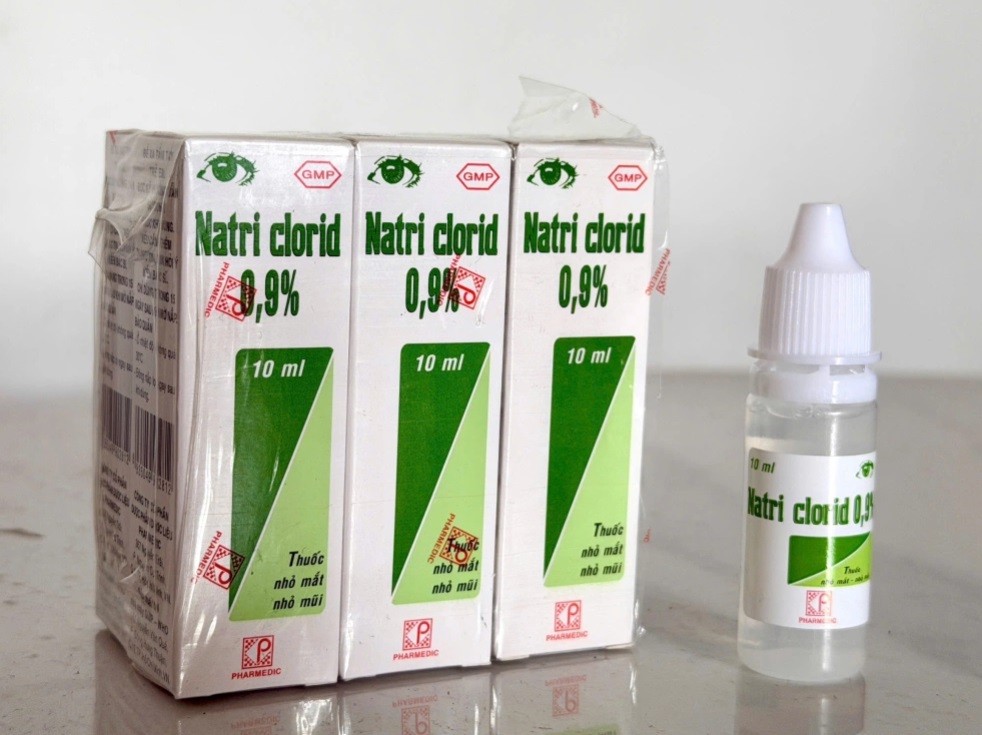
| Thuốc nhỏ mắt Natri clorid 0,9% do Pharmedic sản xuất. Ảnh: Lê Nga |
Cục Quản lý Dược thuộc Bộ Y tế vừa ban hành quyết định thu hồi trên phạm vi toàn quốc đối với một lô thuốc dung dịch nhỏ mắt Natri clorid 0,9% Công ty Cổ phần Dược phẩm Dược liệu Pharmedic sản xuất vì không đạt tiêu chuẩn chất lượng về chỉ tiêu độ trong, vi phạm mức độ 3. Đây là động thái quyết liệt nhằm bảo đảm an toàn cho người sử dụng thuốc, đồng thời tăng cường công tác kiểm tra, giám sát chất lượng dược phẩm lưu hành trên thị trường.
Theo thông tin từ cơ quan chức năng, lô thuốc bị thu hồi là dung dịch nhỏ mắt Natri clorid 0,9%, có số giấy đăng ký lưu hành 893100060724, số lô 10370725, ngày sản xuất 14/7/2025, hạn dùng 14/1/2028, do Công ty Cổ phần Dược phẩm Dược liệu Pharmedic sản xuất.
Theo Viện Kiểm nghiệm thuốc Thành phố Hồ Chí Minh, lô thuốc nói trên không đạt tiêu chuẩn chất lượng về chỉ tiêu độ trong, vi phạm mức độ 3 theo quy định hiện hành. Chỉ tiêu độ trong là một trong những yếu tố quan trọng đối với thuốc nhỏ mắt, bởi sản phẩm sử dụng trực tiếp cho mắt cần bảo đảm tuyệt đối về độ tinh khiết, không lẫn tạp chất gây ảnh hưởng đến sức khỏe người dùng.
Trước thực trạng này, Cục Quản lý Dược yêu cầu các cơ sở kinh doanh, phân phối thuốc trên toàn quốc khẩn trương ngừng kinh doanh, cung cấp và cấp phát lô thuốc nêu trên. Đồng thời, các cơ sở bán buôn, bán lẻ, chuỗi nhà thuốc và cơ sở khám chữa bệnh phải tổ chức thu hồi toàn bộ sản phẩm đã phân phối, trả lại cho đơn vị cung ứng theo đúng quy định.
Đối với doanh nghiệp sản xuất, Cục Quản lý Dược yêu cầu Công ty Cổ phần Dược phẩm Dược liệu Pharmedic lập tức ngừng kinh doanh và tiến hành biệt trữ toàn bộ lô thuốc còn tồn tại cơ sở. Doanh nghiệp phải báo cáo đầy đủ tình hình phân phối sản phẩm đến các cơ sở bán buôn, bán lẻ và các cơ sở khám chữa bệnh có liên quan.
Bên cạnh đó, doanh nghiệp có trách nhiệm chủ trì phối hợp với các tổ chức, cá nhân liên quan để gửi thông báo thu hồi tới toàn bộ hệ thống phân phối đã tiếp nhận lô thuốc này. Việc thu hồi phải được thực hiện nghiêm túc, đồng bộ và hoàn thành trong thời hạn 30 ngày kể từ ngày 11/5 theo yêu cầu của cơ quan quản lý.
Không chỉ dừng lại ở việc thu hồi, doanh nghiệp còn phải thực hiện xử lý toàn bộ lô thuốc vi phạm, chịu mọi chi phí liên quan đến việc thu hồi, tiêu hủy sản phẩm và bồi thường thiệt hại nếu có phát sinh theo đúng quy định của pháp luật.
Các cơ sở khám bệnh, chữa bệnh cũng được yêu cầu ngừng ngay việc kê đơn, cấp phát và sử dụng lô thuốc bị thu hồi. Người dân nếu đang sử dụng sản phẩm thuộc lô thuốc nêu trên cần kiểm tra kỹ thông tin trên bao bì, chủ động ngừng sử dụng và liên hệ với nơi đã mua thuốc để được hướng dẫn đổi trả theo quy định.
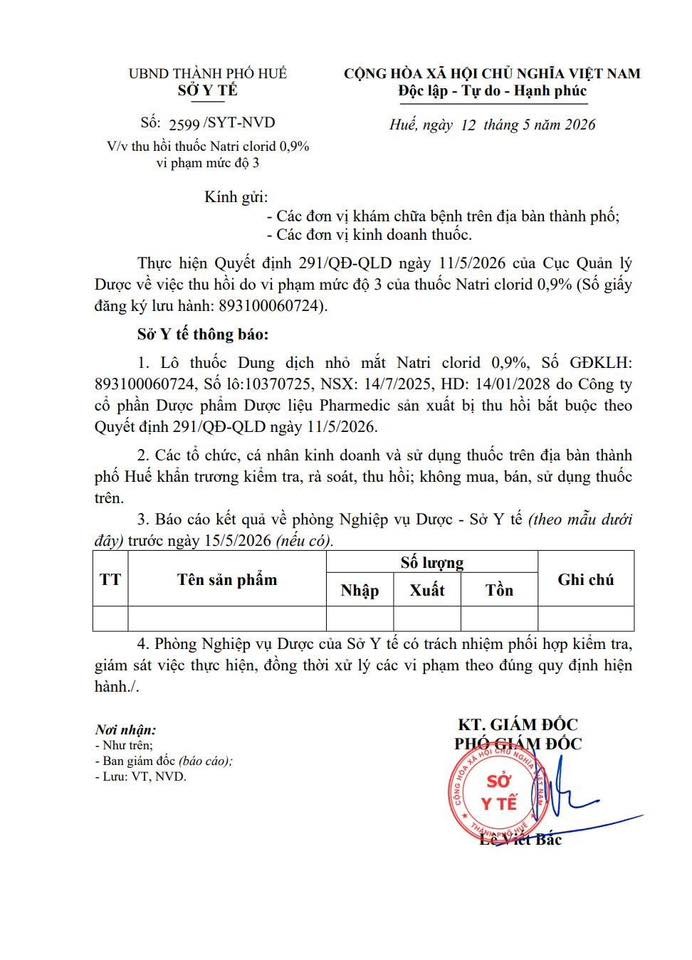 |
| Công văn của Sở Y tế Tp. Huế về việc thu hồi thuốc Natri clorid 0,9% (Số giấy đăng ký lưu hành: 893100060724) vi phạm mức độ 3 |
Việc kịp thời phát hiện và thu hồi lô thuốc không đạt chất lượng thể hiện tinh thần trách nhiệm của ngành Y tế trong công tác bảo vệ sức khỏe nhân dân. Đồng thời, đây cũng là lời cảnh báo đối với các doanh nghiệp sản xuất, kinh doanh dược phẩm cần tuân thủ nghiêm ngặt các quy định về tiêu chuẩn chất lượng thuốc, bảo đảm quyền lợi và sự an toàn cho người tiêu dùng.
Trong bối cảnh nhu cầu sử dụng các sản phẩm chăm sóc mắt ngày càng gia tăng, đặc biệt tại các đô thị lớn, việc kiểm soát chặt chẽ chất lượng thuốc lưu hành trên thị trường là yêu cầu cấp thiết. Các cơ quan chức năng khuyến cáo người dân chỉ nên mua thuốc tại các cơ sở uy tín, được cấp phép hoạt động và cần kiểm tra kỹ thông tin sản phẩm trước khi sử dụng để tránh những rủi ro không mong muốn đối với sức khỏe./.

















